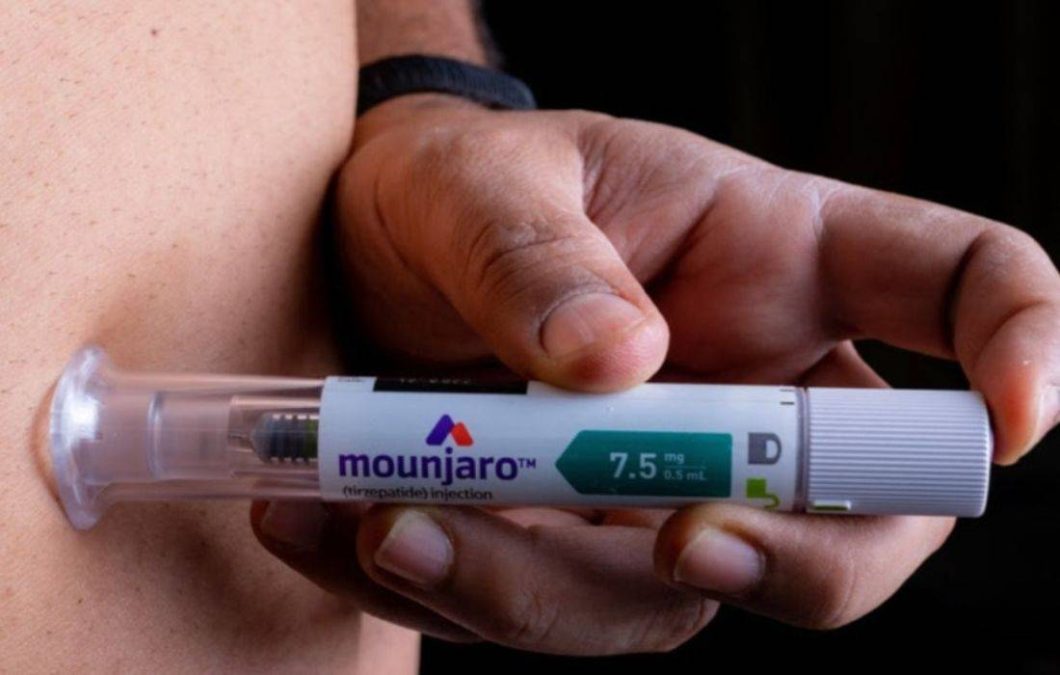
A Agência Nacional de Vigilância Sanitária (Anvisa) autorizou, nesta quarta-feira (22), o uso do medicamento Mounjaro no tratamento de diabetes tipo 2 em pacientes pediátricos a partir dos 10 anos de idade. Até então, a indicação da terapia estava restrita a adultos.
Em comunicado, a Anvisa esclareceu que as demais indicações do fármaco permanecem voltadas ao público adulto, e que a mudança se limita à ampliação da população-alvo para incluir pacientes mais jovens no tratamento do diabetes.
O Mounjaro integra a classe dos agonistas do receptor GLP‑1, grupo de medicamentos que vem sendo referido popularmente como “canetas emagrecedoras”.
Norma sobre manipulação
A diretoria colegiada da Anvisa tem previsto, para a próxima semana, a análise de uma proposta de instrução normativa que estabelecerá procedimentos e requisitos técnicos relativos à manipulação dessas canetas. Segundo a agência, a norma será parte de um conjunto de medidas regulatórias e de fiscalização inseridas no plano de ação anunciado no último dia 6, destinado a aprimorar o controle sobre esse tipo de medicamento.
Grupos de trabalho

Na semana anterior, a Anvisa publicou portarias criando dois grupos de trabalho para apoiar a atuação da autarquia no controle sanitário e na segurança de pacientes que utilizam as canetas com agonistas de GLP‑1. A Portaria 488/2026 instituiu o primeiro grupo, composto por representantes do Conselho Federal de Farmácia (CFF), do Conselho Federal de Medicina (CFM) e do Conselho Federal de Odontologia (CFO).
A Portaria 489/2026 criou o segundo grupo, responsável por acompanhar e avaliar a execução do plano de ação proposto pela Anvisa e por oferecer subsídios à diretoria colegiada por meio da proposição de medidas de aprimoramento.
As medidas anunciadas pela agência buscam reforçar a regulação e a fiscalização dos medicamentos da classe dos agonistas do receptor GLP‑1, ao mesmo tempo em que ampliam a faixa etária para a qual o Mounjaro pode ser prescrito no tratamento do diabetes tipo 2.
Com informações de Maispb





